sp2杂化:同一原子内由1个ns轨道和2个np轨道参与的杂化。
例如,在乙烯(C₂H₄)分子中有碳碳双键(C=C),碳原子在形成乙烯分子时,每个碳原子的2s轨道与两个2p轨道发生sp2杂化,形成3个杂化轨道。
sp3杂化:同一原子内由1个ns轨道和3个np轨道参与的杂化。
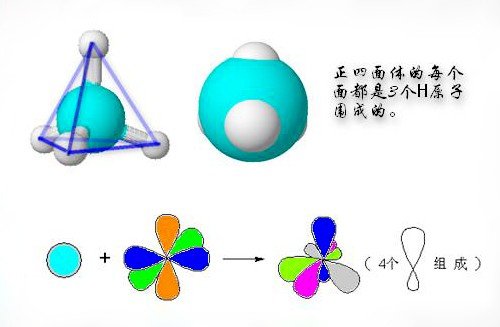
例如,甲烷(CH₄)的形成,基态C原子只有两个未成对电子 ,在形成甲烷时,在H的影响下,C的1个2s轨道和3个2p轨道进行sp3杂化,形成4个sp3杂化轨道。
扩展资料
判断
1、判断中心原子的孤电子对的数量;
2、找出与中心原子相连的原子数(即形成的σ键的数量);
3、若二者相加等于2,那么中心原子采用SP杂化;若等于3,那么中心原子采用SP2杂化;若等于4,那么中心原子采用SP3杂化。
局限性
最初原子轨道的杂化概念完全是人造的,是为了解释 CH₄—四面体这类的现象。后来分子轨道理论出现,原子轨道的杂化就自然而然的被解释了——只不过是一种同原子的原子轨道的重新线性组合。
同时,分子轨道理论也表明了这种组合(杂化)没有实际上的意义,而且有时会引起混乱。譬如:在杂化理论中,CH₄中的八个成键电子是在同一种sp3轨道能级上。
但其实,它们是分在两个不同的能级上的(试验和分子轨道理论都表明了这一点)。但由于杂化概念的方便,特别是在有机化学中被用来表示一个原子在分子中的几何环境。所以,杂化轨道仅被用来描述几何形状或环境。
参考资料来源:百度百科--sp2杂化
参考资料来源:百度百科--sp3杂化



